细胞的活动高度依赖于活性氧(ROS)信号分子,其中超氧阴离子(O2•−)和过氧化氢(H2O2)共同调节细胞凋亡和氧化应激等生物学过程,实现O2•−和H2O2的同时鉴定具有重要意义,但在复杂环境下同时检测活细胞释放的O2•−和H2O2仍面临较大挑战。
近日,我院生化传感团队李长明/郭春显教授团队最新研究成果发表在传感领域知名期刊ACS Sensors (IF=9.618)上,相关成果题目为“Interfacial Regulation of ZIF-67 on Bacteria to Generate Bifunctional Sensing Material on Chip for Qualifying Cell-Released Reactive Oxygen Species”。史转转博士为第一作者,郭春显、李长明教授为通讯作者,我校为第一通讯单位。
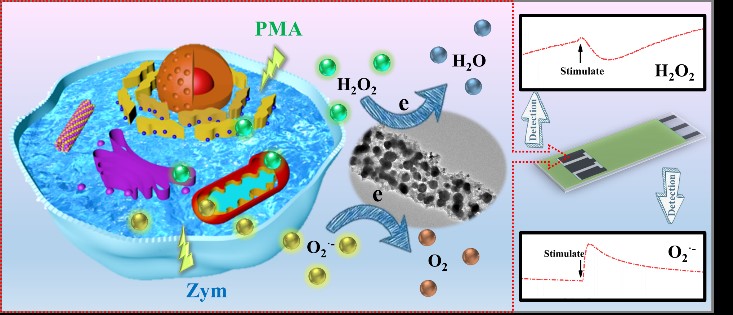
该研究成果从分子传感界面定向构筑的角度出发,设计合成了一种双功能仿生酶传感材料,通过界面调节ZIF-67对细菌的原位修饰获得了钴纳米颗粒/氮掺杂多孔碳纳米棒(Co/N-doped CNRs) 定向构筑了双功能分子传感界面。进一步,基于印刷技术构建了电化学传感芯片实现了对细胞释放O2•−和H2O2的同时检测。Co/N-doped CNRs具有独特的多孔结构和显著增大的比表面积,其中Co纳米颗粒提供了丰富的活性位点。利用双功能Co/N-doped CNRs制备电化学传感芯片,其响应时间短(O2•−为0.5 s, H2O2为1.9 s),检出限低(O2•−为0.69 nM, H2O2为2.25 μM),灵敏度高(O2•−为792.30 μA·μM−1·cm−2, H2O2为153.91 μA·mM−1·cm−2),优于目前报道的双功能仿生酶。
该工作的开展获得了国家重点研发计划(2021YFA0910403)、国家自然科学基金面上项目(NO.21972102)等支持。